> 财商 » 正文
博腾生物热烈祝贺来恩生物mRNA TCR-T细胞疗法获NMPA IND默示许可
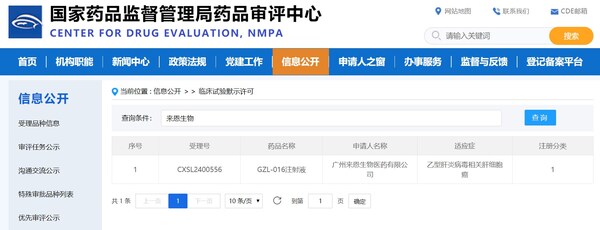
苏州2024年11月14日 /美通社/ -- 2024年11月12日,广州来恩生物医药有限公司(以下简称"来恩生物")所提交的"GZL-016注射液"新药临床试验申请(IND)获得国家药品监督管理局默示许可。GZL-016注射液是一款mRNA TCR-T细胞疗法,适应症为乙型肝炎病毒相关肝细胞癌,此次获批也标志着TCR-T细胞疗法用于实体瘤治疗领域的一项重要突破。博腾生物对此表示热烈祝贺。
GZL-016注射液通过mRNA编码T细胞受体(TCR), 靶向乙肝病毒表面抗原,因此经体外改造的T细胞被赋予了特异性识别并杀伤HBV相关肝细胞癌的能力。这款自体T细胞疗法利用mRNA瞬时表达的特性,结合多次输注的临床治疗方案,旨在保证患者用药安全性的同时带来了令人期待的疗效。在治疗前,患者无需进行清淋,这进一步提高了治疗的安全性和可及性。本次IND获批,进一步证明了来恩生物的研发与创新实力。
博腾生物作为来恩生物的CDMO合作伙伴,和来恩生物密切合作,为该项目提供了药学研究相关的服务,最大限度的保证了项目交付质量和周期。双方团队紧密合作,极大地加快了GZL-016注射液的IND申请进程。
来恩生物拥有的这款自体T细胞治疗产品是全球首款(First-in-Class)针对乙肝病毒表面抗原,用于治疗乙肝相关肝细胞癌的TCR-T细胞治疗产品。这款产品此前已经获得美国FDA批准的全球第一个1b/2期IND临床试验批件,并且获得了FDA的快速通道认定。博腾生物祝愿来恩生物未来在mRNA编码TCR-T疗法领域取得更多新进展,惠及更多患者。
本文标签: